
Die Enzymtrainerin
Die Biochemikerin und ihr Team optimieren Enzyme, die helfen sollen, antibiotikaresistente Keime oder Plastikabfall zu bekämpfen. Rebecca Buller leitet die ZHAW-Fachstelle Biokatalyse und Prozesstechnologie.
Mittags auf dem ZHAW-Campus Reidbach in Wädenswil: In den Bioreaktoren der Fachstelle Biokatalyse und Prozesstechnologie werden literweise oder in kleinem Massstab Escherichia-coli-Bakterien gerührt oder geschüttelt. Die Kolibakterien sind mit einem Bauplan für die gewünschten Enzyme versehen und sollen sich vermehren, um so grössere Mengen der Biokatalysatoren zu produzieren. In speziellen Verfahren werden die Enzyme später abgetrennt und sollen als Katalysatoren bei chemischen Prozessen eingesetzt werden.
Während Rebecca Buller, Leiterin der Fachstelle, die Journalistin und Fotografen durch die Labore ihres Teams führt, erzählt sie von der jungen und aufstrebenden Disziplin Biokatalyse, die angetreten ist, chemische Prozesse noch wirkungsvoller und nachhaltiger zu machen: «In der westlichen Welt haben wir eine sehr hohe Lebensqualität erreicht.» Die Gesellschaft stehe jetzt aber vor neuen Herausforderungen: «Wie kann eine nachhaltige Nahrungsmittel- und Energieversorgung aussehen, welche Antworten gibt es auf nach wie vor offene Gesundheits- oder Umweltfragen? Hier will die Biokatalyse zu Lösungen beitragen.»
Enzyme – die Multitalente aus der Natur
Dabei setzt die Disziplin auf Enzyme, die Multitalente aus der Natur. Sie helfen, chemische Reaktionen zu beschleunigen, giftige Reagenzien und Lösungsmittel zu ersetzen und nicht zuletzt Reaktionen überhaupt erst zu ermöglichen, die ohne sie gar nicht erreichbar wären. Sie können durch Fermentation in grossen Mengen hergestellt werden, wirken sehr spezifisch, sind biologisch abbaubar und im Gegensatz zu Edelmetallen, die bisher häufig als Katalysatoren eingesetzt werden, nicht von grossen Preisschwankungen betroffen. «Vor allem die Geruchs- und Geschmacksstoffbranche, die Pharma- sowie die agrochemische Industrie haben die Stärken der Biokatalyse erkannt», betont die Professorin für Chemische und Biotechnologische Methoden, Systeme und Prozesse.
«Enzyme optimieren ist wie Hochleistungssport.»
Nach der Besichtigung der Labore führt sie die Besucher in ihr Büro. Anhand von Modellen auf ihrem Laptop erklärt sie, was die Biokatalyse genau macht: «Weil die wenigsten Enzyme so eingesetzt werden können, wie sie in der Natur vorkommen, werden sie durch die sogenannte gerichtete Evolution für industrielle Anwendungen optimiert.» Dank der rasanten Entwicklung in der Molekularbiologie, insbesondere im Bereich Gensequenzierung und -synthese, können Enzyme immer einfacher und preisgünstiger optimiert werden. Das führte in den vergangenen 20 Jahren zu einem Aufschwung der Disziplin. Im Jahr 2018 erhielt die US-Forscherin Frances Arnold den Chemie-Nobelpreis für Arbeiten zur gerichteten Evolution von Enzymen.
Erst Talentsuche, dann das Training
Rebecca Buller vergleicht das Optimieren von Enzymen mit dem Profisport: «Im Hochleistungssport werden zuerst Talente gesucht, bevor sie dann durch Training zu Spitzenleistungen gebracht werden.» Auf der Suche nach einem industriell einsetzbaren Enzym identifizieren die Fachleute ebenfalls zuerst mögliche Kandidaten, die prinzipiell in der Lage sein müssen, das gewünschte Molekül herzustellen. «Dann folgt das Training, bei dem unsere Forscherinnen und Forscher das Enzym mittels der gerichteten Evolution zu Hochleistungen bringen.» Wie schwierig das Training ist, verdeutlicht sie an einem Rechenbeispiel: Enzyme bestehen aus 20 verschiedenen Aminosäuren, die wie Legobausteine aneinandergereiht sind. Diese Bausteinketten sind meist zwischen 200 und 400 Aminosäuren lang. Damit ein Enzym genau so arbeitet, wie die Forscherinnen und Forscher es möchten, müssen häufig einige Aminosäure-Bausteine ausgetauscht werden. Würde man nur zwei davon gleichzeitig ändern, wären 400 neue Varianten möglich, bei fünf gibt es bereits 3,2 Millionen Möglichkeiten. «All diese Kombinationen zu testen, wäre für einen Menschen schlicht unmöglich.»
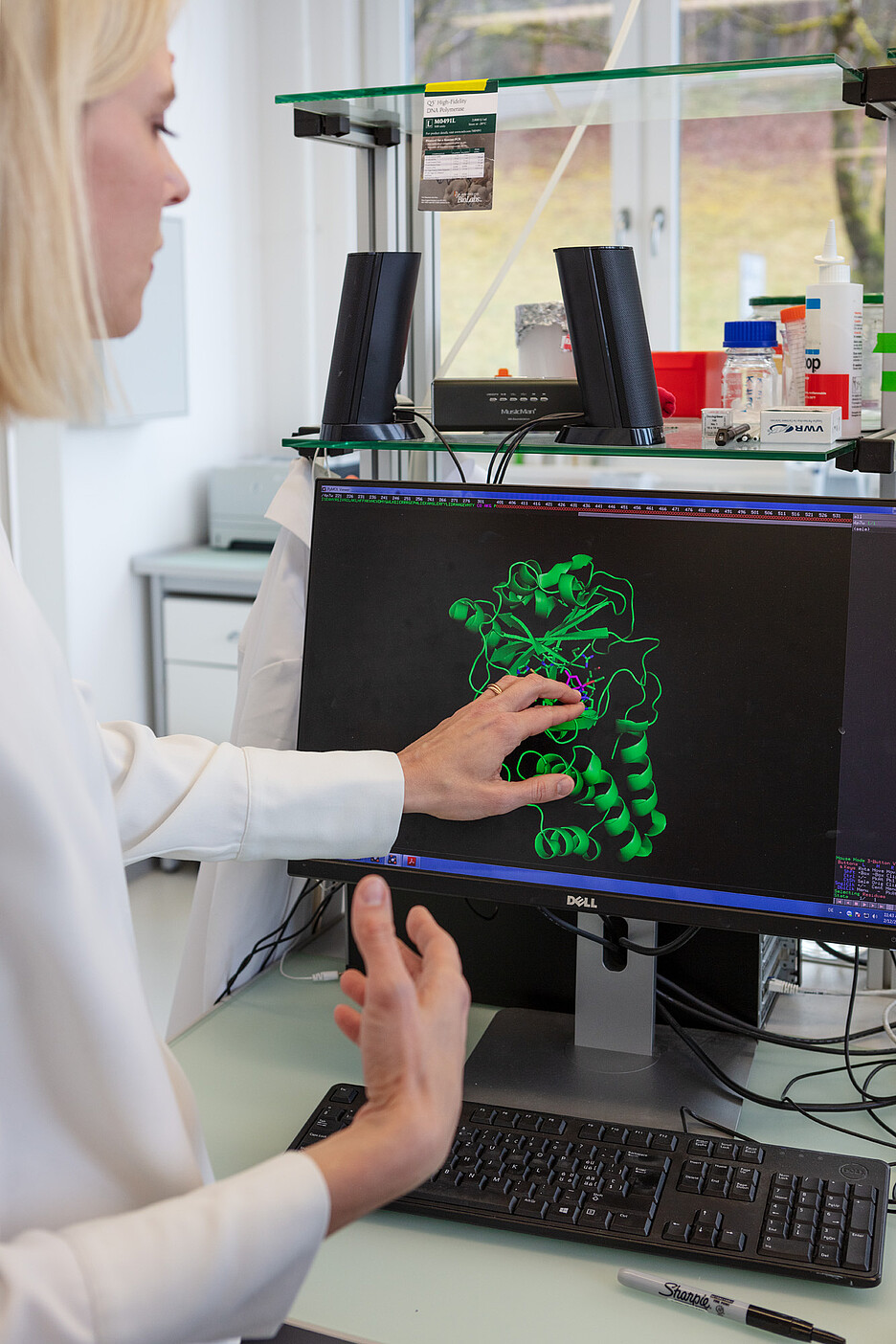
«Die Meisterschaft ist dann gewonnen, wenn ein optimiertes Enzym die Produktherstellung ermöglicht.»
Deshalb setzt ihre Fachstelle auf Automatisierung und Künstliche Intelligenz. Computergestützte Modelle zur Vorhersage werden entwickelt. «Das System lernt dabei, wie sich bestimmte Aminosäure-Kombinationen auf die Enzymaktivität auswirken – und so unterstützt der Algorithmus uns bei der Suche nach der idealen Bausteinkombination.» Entscheidend ist dann noch eine erfolgsversprechende «Spiel-Strategie»: Bei welchen Temperaturen, welchem pH-Wert oder welcher Enzymmenge verläuft die gewünschte Reaktion bestmöglich? «Die Weltmeisterschaft haben wir dann gewonnen, wenn ein optimiertes Enzym die Herstellung des gewünschten Produkts erleichtert oder überhaupt erst ermöglicht.»
Enzymen auf die Sprünge helfen
Im «Trainingscamp» von Rebecca Buller befinden sich derzeit unter anderem Enzymkandidaten, die helfen sollen, Plastikabfall abzubauen. Im Jahr 2016 wurde ein solches Enzym in einer Bodenprobe einer japanischen Recyclinganlage entdeckt. «Es ist nicht gerade das schnellste Enzym der Welt», scherzt Rebecca Buller. Deshalb wollen sie und ihr Kooperationspartner, die ETH Zürich, dem Enzym durch Algorithmus-gestützte gerichtete Evolution auf die Sprünge helfen. Gefördert wird das Projekt im Rahmen des nationalen Forschungsschwerpunkts «Catalysis».

Bei der Suche nach dem «Best-Talent» zur Herstellung von Wirkstoffen gegen antibiotikaresistente Keime, kooperiert ihre Fachstelle mit Fachleuten der Universität Bern im Rahmen des Sonderprogramms «Bridge» der Förderagentur Innosuisse des Bundes und des Schweizerischen Nationalfonds. «Multiresistente Bakterien verursachen heute viel Leid und hohe Kosten», erklärt Rebecca Buller, «deshalb wollen wir zur Entwicklung neuer Wirkstoffe beitragen.» Als Mutter zweier kleiner Kinder war sie selbst schon froh, wenn Antibiotika bei Infektionen halfen und das Fieber zurückging. Deshalb setzt sie sich dafür ein, dass es auch künftig selbstverständlich sein soll, bakteriell verursachte Infektionen mit Antibiotika bekämpfen zu können. Im Fokus dieser Arbeiten stehen Peptide – vielversprechende aus Aminosäuren aufgebaute organisch-chemische Verbindungen. Sie werden im Körper jedoch schnell als Fremdstoffe erkannt und abgebaut. Das Forschungskonsortium untersucht deshalb, ob und wie die Peptide mit Hilfe von enzymatischen Transformationen so stabilisiert werden können, dass neu Peptidwirkstoffe entstehen, die dann eine Wirksamkeit gegen resistente Bakterienstämme entfalten könnten.
Von der Natur lernen
Die Faszination für die Chemie und die Enzyme führt Rebecca Buller, nicht nur auf ihre gute Chemielehrerin zurück: «Ich war schon als Kind sehr neugierig und mathematisch, naturwissenschaftlich interessiert.» Aufgewachsen in einer deutschen Kleinstadt in der Nähe von Münster, studierte sie an der Westfälischen Wilhelms-Universität Chemie. «Mich fasziniert, wie diese Disziplin unser Leben so stark bestimmt, von der Ernährung und der Kleidung über Farben bis zur Speicherung von Energie und vielem mehr.» Während des Studiums wurde ihr klar: «Die Natur betreibt die bessere Chemie. Wir können einiges von ihr lernen.»
«Die Natur macht die beste Chemie.»
Spricht sie über Enzyme, gerät sie regelrecht ins Schwärmen: «Enzyme sind solch perfekte, kleine Maschinen.» Im Studium lernte sie moderne molekularbiologische Methoden kennen und begann, sich für die Arbeit mit massgeschneiderten Enzymen zu begeistern. Während ihres Studienjahrs an der University of California in Santa Barbara konnte sie zum ersten Mal intensiv in diesem wissenschaftlichen Feld experimentieren. Für ihre Doktorarbeit an der ETH Zürich widmete sie sich der gerichteten Evolution von Enzymen und konnte Ergebnisse ihrer Arbeit in der renommierten Wissenschaftszeitschrift «Nature» publizieren. «Später wollte ich nicht nur verstehen, wie Prozesse auf molekularer Ebene funktionieren, sondern auch, wie man dieses Wissen für Anwendungen in der Industrie nutzen kann», sagt die heutige Professorin. Sie nahm daher eine Stelle beim international tätigen Schweizer Aromen- und Duftstoff-Hersteller Firmenich an und leitete ein Labor in Genf. Im Eilzugtempo lernte sie Französisch: «Ich konnte nämlich zu Beginn kein Wort – aber im Labor müssen wir in jeder Hinsicht die gleiche Sprache sprechen», sagt Rebecca Buller, die heute mit ihrer Familie im Limmattal lebt.

«Mich fasziniert, wie die Chemie unser Leben so stark bestimmt.»
Nach vier Jahren in dem Westschweizer Unternehmen vermisste sie das akademische Umfeld und die Zusammenarbeit mit Studierenden. Eine Stellenausschreibung für den Aufbau eines Kompetenzzentrums Biokatalyse an der ZHAW weckte sofort ihr Interesse: «Ich mag es, mit interdisziplinären Teams zu arbeiten und etwas von Grund auf zu gestalten», sagt Rebecca Buller und ergänzt: «Mit den neuen Erkenntnissen, die wir in unserer Forschungsgruppe erzielen, können wir nicht nur die Grundlagenforschung voranbringen, sondern sie gleichzeitig auch in Zusammenarbeit mit verschiedenen Firmen testen.» Seit ihrem Wechsel an die ZHAW sind fünf Jahre vergangen. Sie hat inzwischen die Fachstelle Biokatalyse in der Schweiz zur wichtigsten Adresse in der angewandten Biokatalyse gemacht. Hatte sie zu Beginn eine Mitarbeiterin, arbeiten hier heute 15 wissenschaftliche Mitarbeitende, technische Angestellte und PhD-Studierende. Sie konnte bedeutende Forschungsprojekte akquirieren, gefördert von Innosuisse, dem Schweizerischem Nationalfonds und Industriepartnern.
Die Netzwerkerin
Wie ihre Enzyme wirkt auch die Professorin bisweilen wie ein Katalysator und bringt Menschen zusammen, die ohne ihr Zutun schwerer oder gar nicht zusammengefunden hätten. Das war so beim «Innovationsraum Biokatalyse», bei dem Rebecca Buller im Auftrag und mit zwei Millionen Fördermitteln des Bundes vor drei Jahren dieses Netzwerkprojekt startete. Dabei wurden nicht nur zahlreiche biokatalytische Forschungsvorhaben erfolgreich finanziert und Forschende vernetzt, sondern die Biokatalyse auch besser im Studium verankert. Nicht zuletzt gründete sie die Plattform Swiss Women in Chemistry (SWC) mit, ein Netzwerk für Chemikerinnen verschiedener Altersstufen und Tätigkeitsbereiche, welches auch Mentoring-Programme für junge Forscherinnen organisiert.
Für die Natur begeistert sich Rebecca Buller nicht nur beruflich, sondern auch privat. Mit ihrer Familie verbringt sie ihre Freizeit gerne in den Schweizer Bergen. Und während sie erzählt, deutet sie aus ihrem Bürofenster, wo die Alpen an dem Tag zum Greifen nah erscheinen, während im Labor die Kolibakterien geschüttelt werden.





0 Kommentare
Sei der Erste der kommentiert!